Page 13 - eAB12002_Arduino 微電腦應用實習_課本PDF
P. 13
第 1 章 電學概論
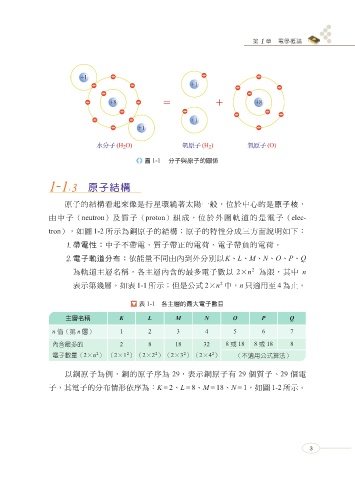
圖 1-1 分子與原子的關係
-
1 1. 3 原子結構
原子的結構看起來像是行星環繞著太陽一般,位於中心的是原子核,
由中子(neutron)及質子(proton)組 成,位於外圍軌道的是電子(elec-
tron),如圖 1-2 所示為銅原子的結構;原子的特性分成三方面說明如下:
帶電性:中子不帶電、質子帶正的電荷、電子帶負的電荷。
電子軌道分布:依能量不同由內到外分別以K、L、M、N、O、P、Q
為軌道主層名稱,各主層內含的最多電子數以 2×n 為限,其中 n
2
2
表示第幾層,如表 1-1 所示;但是公式 2×n 中,n 只適用至 4 為止。
表 1-1 各主層的最大電子數目
主層名稱 K L M N O P Q
n 值(第 n 層) 1 2 3 4 5 6 7
內含最多的 2 8 18 32 8 或 18 8 或 18 8
2
2
2
2
2
電子數量(2×n ) (2×1 ) (2×2 ) (2×3 ) (2×4 ) (不適用公式算法)
以銅原子為例,銅的原子序為 29,表示銅原子有 29 個質子、29 個電
子,其電子的分布情形依序為:K =2、L =8、M =18、N =1,如圖 1-2 所示。
3