Page 21 - CB01302_汽車學-汽車電學篇
P. 21
第一章 電 瓶
電瓶在充電時,係將電能轉換成化學能,儲存在正負極板內,其
化學反應如下:
PbO 2+2H 2SO 4+Pb
PbSO 4+2H 2O+PbSO 4
正極板 負極板 正極板 負極板
由此化學式可知,電瓶在充電時,正負極板中之硫酸根會離開進
入電水內,與電水中的氫分子結合成硫酸,而使電水之比重升高,而
電水中的氧分子也會進入正極板內形成過氧化鉛(PbO 2),負極板因硫
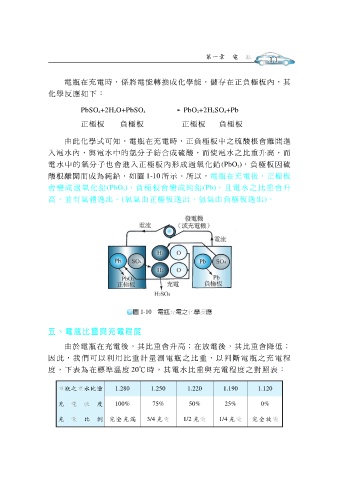
酸根離開而成為純鉛,如圖 1-10 所示。所以,電瓶在充電後,正極板
會 變成過氧化鉛(PbO 2),負極板 會 變成純鉛(Pb),且電水之比 重會 升
高,並有氣體逸出。(氧氣由正極板逸出,氫氣由負極板逸出)。
圖 1-10 應
電瓶充
化學反
電之
五、 電瓶 比重 與 充電 程度
由於電瓶在充電後,其比重會升高;在放電後,其比重會降低;
因 此,我們 可以 利用比 重計 量 測 電瓶之比 重,以 判斷 電 瓶之充電程
度,下表為在標準溫度 20℃時,其電水比重與充電程度之對照表:
1.280 1.250 1.220 1.190 1.120
電瓶之電水比重
100% 75% 50% 25% 0%
充 電 程 度
3/4 充電 1/2 充電 1/4 充電 完全放電
電
比
充
例完全充滿