Page 12 - eEC00620_化工裝置 II_課本PDF
P. 12
化工裝置 II
9-1
、 :分別為平衡時蒸氣中 A、B 成分之分壓(mmHg 或 Pa)。
、 :分別為同溫下純物質 A、B 之飽和蒸氣壓(mmHg 或 Pa)。
、 :分別為理想溶液中成分 A、B 之莫耳分率。
習慣上我們將較容易揮發的成分在蒸氣中之莫耳分率以 表示,在液體
中之莫耳分率以 代表。符合拉午耳定律的溶液稱為理想溶液(ideal solution),
如苯-甲苯溶液。而純物質的蒸氣壓( 、 )與溫度有關,在定溫時,蒸
氣壓愈高,則沸點愈低。表 9-1 為苯-甲苯溶液在不同溫度時的蒸氣壓。
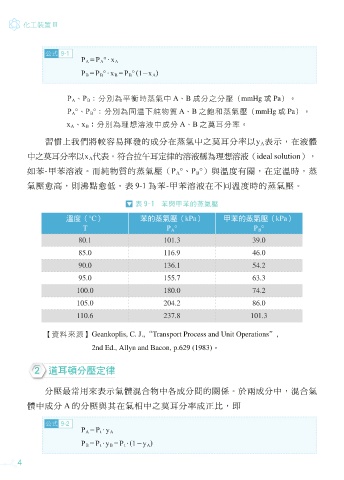
表 9-1 苯與甲苯的蒸氣壓
溫度(°C) 苯的蒸氣壓(kPa) 甲苯的蒸氣壓(kPa)
T
80.1 101.3 39.0
85.0 116.9 46.0
90.0 136.1 54.2
95.0 155.7 63.3
100.0 180.0 74.2
105.0 204.2 86.0
110.6 237.8 101.3
【資料來源】Geankoplis, C. J.,“Transport Process and Unit Operations”,
2nd Ed., Allyn and Bacon, p.629 (1983)。
2 道耳頓分壓定律
分壓最常用來表示氣體混合物中各成分間的關係。於兩成分中,混合氣
體中成分 A 的分壓與其在氣相中之莫耳分率成正比,即
9-2
4